引言
在过去十年的研究过程中,基因传递到中枢和外周神经系统(CNS和PNS)的进步极大地促进了神经科学的研究进展,并有可能将相关的研究成果推向临床,为治疗神经系统疾病提供新的疗法。然而,跨物种的非侵入性基因递送方式的研究空白,极大地限制了神经科学相关研究向临床的转化。
在病毒载体递送基因的相关研究中,最有临床转化潜力的是腺相关病毒(AAV),AAV具有高稳定性、长期表达和低免疫原性的特点,深受神经科学工作者的喜爱。但是大部分AAV均需要通过侵入性手术的方式进行注射,并且由于血脑屏障的存在,通过静脉注射的AAV基本上不能在中枢神经系统和外周神经系统表达。最新的研究成果发现AAV-PHP.eB可以高效的通过血脑屏障,将基因递送到中枢系统;而AAV-PHP.S则偏向于表达在外周神经系统中,但是这两类病毒载体仅在小鼠中起效。
对于非人灵长类动物模型的基因递送手段的缺乏,严重地制约了基础研究向临床研究的转化进程。而基因治疗在解决与中枢和外周神经系统相关的神经病理学方面具有巨大的前景。因此开发跨物种的有效和非侵入性基因传递载体是一个迫切需求。研究人员需开发出一类跨物种在啮齿类动物和非人灵长类动物中稳定性表达,并且透过血脑屏障的AAV载体,这将有利于推进基因治疗的临床前研究。
加州理工学院Chen X等人进化出一个AAV9衣壳变体家族,包括MaCPNS1和MaCPNS2。啮齿类动物(小鼠和大鼠)中系统注射AAV-MaCPNS1或AAV-MaCPNS2即可有效转导PNS,并能解析PNS功能和无创调控PNS。另外,这两种载体还可以有效地将基因同时传递到非人灵长类动物(恒河猴和狨猴)的PNS和CNS。
结果
01
跨物种并且透过血脑屏障的病毒衣壳的开发
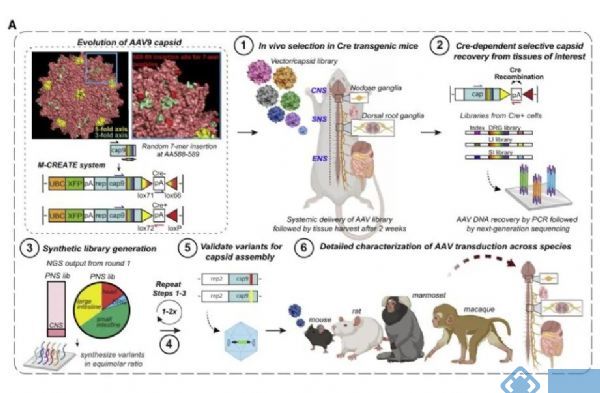
为了制备衣壳多样化的病毒载体,作者通过在AAV9衣壳位点A588到589之间随机插入一个七肽,来制备多样性的AAV9病毒衣壳。之后将制备的病毒载体通过尾静脉的方式,注射到不同品系的转基因鼠中,筛选出能感染神经元的病毒衣壳。通过两轮筛选,研究人员从6300个变体中筛选出具有神经元噬性的病毒衣壳,随后通过UMAP算法(uniform manifold approximation and projection algorithm;统一流形近似与投影)鉴定出2个高选择性在外周神经系统和中枢神经系统中表达的新的病毒衣壳AAV-MaCPNS1和AAV-MaCPNS2。
图1. AAV-MaCPNS1/2的开发过程
02
AAV-MaCPNS1/2感染啮齿类动物的外周神经系统
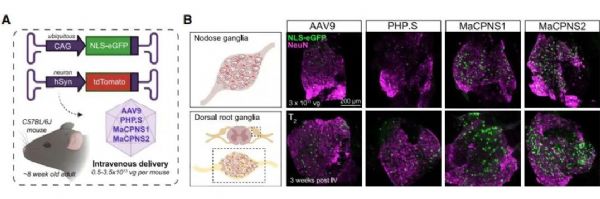
目前基础研究使用的病毒载体中,特异性干预外周神经系统的载体并不多见,AAV-PHP.S基本是唯一的选择。为了测试AAV-MaCPNS1/2对外周神经系统的噬性,研究人员通过尾静脉注射将AAV-PHP.S、AAV-MaCPNS1和AAV-MaCPNS2注入小鼠体内,发现在尾静脉注射相同病毒剂量的情况下,AAV-MaCPNS1/2在外周神经系统的结状神经节、背根神经节和肠神经元的表达均比AAV-PHP.S高出2倍以上。体现出AAV-MaCPNS1/2在感染啮齿类动物外周系统的优越性。
图2. AAV-MaCPNS1/2在结状神经节、背根神经节的表达效果优于AAV-PHP.S
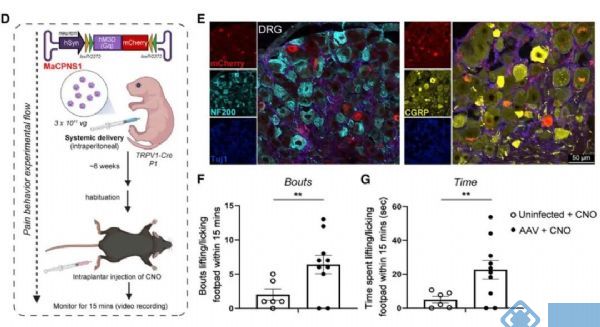
既然AAV-MaCPNS1/2在啮齿类外周神经系统有优越的表达特性,那么有没有可能结合遗传改造手段监测和干预外周神经系统的神经元呢?研究人员将基因编码的钙指示剂(GECI-jGCaMP8s)的相关元件整合到AAV-MaCPNS1(尾静脉注射),发现在肠道注入葡萄糖后,能监测到结状神经节神经元活性变化。同样的将化学遗传学激活元件[DIO-HM3D(Gq)]整合到AAV-MaCPNS1(尾静脉注射),使用CNO激活DREADD后,在TRPV1(感受温度和疼痛的离子通道蛋白)-Cre小鼠上检测到明显的疼痛样行为(激活背根神经节中TRPV1+神经元)。体现出AAV-MaCPNS1在监测和调控外周神经系统的相关研究中的优越性。
图3. 尾静脉注射AAV-MaCPNS1激活背根神经节中TRPV1+神经元引起疼痛
03
AAV-MaCPNS1/2感染非人灵长类动物外周和中枢神经系统
为了研究静脉注射AAV-MaCPNS1/2在非人灵长类动物中的表达效率。研究人员通过尾静脉注射将AAV-MaCPNS1/2注射到狨猴和恒河猴的体内,以临床研究喜爱使用的AAV9作为对照组。发现AAV9在背根神经节和肠神经处不表达,而AAV-MaCPNS1/2稳定表达。此外AAV-MaCPNS1/2在中枢系统的表达效率是AAV9的数十倍以上,包括脊髓、皮层、丘脑、小脑、脑干等多个脑区。体现出AAV-MaCPNS1/2在非人灵长类动物的外周表达和中枢表达的优越性。
图4. AAV9和AAV-MaCPNS1/2在狨猴背根神经节和小肠的表达
图5. AAV9和AAV-MaCPNS1/2在狨猴大脑不同区域的表达
结论
总而言之,本文通过定向进化的手段获得AAV-MaCPNS1/2两类病毒衣壳,该病毒填补了啮齿类动物的外周神经系统监测和干预手段的空白,并且通过静脉注射在非人灵长类动物的中枢神经系统有良好的表达特性,极具基础研究和临床转化价值。
图6. 总结图. AAV-MaCPNS1/2在啮齿类动物和非人灵长类动物的表达情况
我司可提供MaCPNS1和MaCPNS2血清型病毒载体,部分列表如下:
更多产品请联系我们!
扫码下载原文
我司重磅推出环路示踪,光遗传,钙记录,膜片钳,电生理等动物实验服务!
公司相关业务:
神经环路示踪病毒载体、基因编辑(敲入、敲除、点突变、敲低)、基因过表达/干扰服务、行为学小鼠模型构建、干细胞诱导分化、整包服务等。