中南大学湘雅二医院陈林老师长期从事口腔癌的发生发展机制及治疗。近期,其实验室通过Arraystar circRNA芯片发现一种调控口腔鳞状细胞癌发生发展的circRNA分子—circRNA_100290。CircRNA_100290通过内源竞争结合miR-29,从而解除miR-29对CDK6的抑制,促进口腔鳞状细胞癌的发生发展。该成果发表在Nature子刊Oncogene(IF=7.932)。(芯片由康成生物提供技术服务)。
研究背景
口腔鳞状细胞癌(OSCC)是世界发病率排行前八的恶性肿瘤之一,发病率和致死率并没有因为手术技术的提高而减少,是公认的卫生难题。在过去十年里,miRNA、lncRNA都被证明在癌症的发生过程中有很重要的作用,一些文章中特别介绍了miRNA可以作为OSCC的调控因子起作用;但动物体内广泛存在的circRNA,在肿瘤的发生和进展中的研究并不十分多见,尤其是OSCC。目前一些circRNA如:ciRs-7、sry和circHIPK3的ceRNA机制研究都已经得到证明。本文通过研究OSCC的circRNA和mRNA表达谱,得到差异表达的circRNA_100290,通过ceRNA机制分析,得到相应靶基因CDK6,并证明其通过内源性竞争结合miR-29,从而调控CDK6的表达,促进OSCC的发生发展,为OSCC的治疗提供潜在靶标。
研究思路
为了探究circRNA在OSCC发生和发展的作用,本文使用Arraystar circRNA芯片,分析OSCC及NCMT样本,分析circRNA表达谱,发现共有280个circRNA表达发生显著表达,其中139个circRNA上调,141个circRNA下调,从上调最显著的10个circRNA中选出circRNA_100290, q-PCR验证circRNA_100290确实在OSCC组织中表达显著上调。
已经报道的circRNA多是通过ceRNA机制发挥功能,作者更深一步挖掘circRNA_100290的分子机制,通过miRNA数据库:Targetscan、miRanda和RNA22,预测circRNA_100290靶基因, 得到评分最高的3个microRNA:miR-29b-3p,miR-29c-3p,miR-29a-3p及最可能相关的靶基因CDK6,该基因是细胞周期相关蛋白,且在表达谱芯片中显著上调。作者通过敲低OSCC细胞系circRNA_100290的表达,发现这些细胞中CDK6表达也显著下调,证明CDK6的表达受到circRNA_100290的调控。CDK6在细胞周期中有非常重要的作用,能促进细胞进入DNA合成的S期,通过MTT和BrdU实验证明,敲除circRNA_100290,或者使用miR-29的类似物,都能显著降低CAL27细胞的增殖。作者同时在in vivo水平进行了验证,将正常HN4细胞和circRNA_100290敲除的HN4细胞植入小鼠体内,3周后检测发现,未经敲除的小鼠体内肿瘤体积的增加量多于circRNA_100290敲除的小鼠,通过荧光素酶实验证明miR-29能在细胞内直接结合circRNA_100290和CDK6。
技术路线
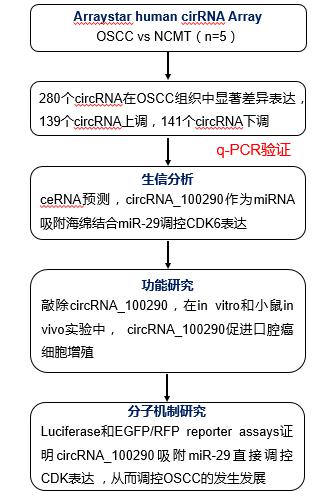
结果展示
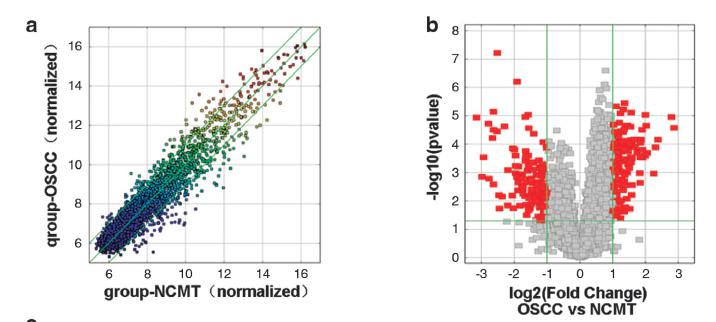
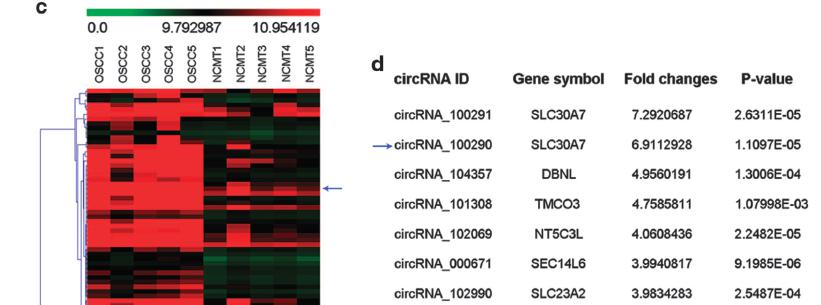
图1:circRNA芯片筛选差异显著circRNA
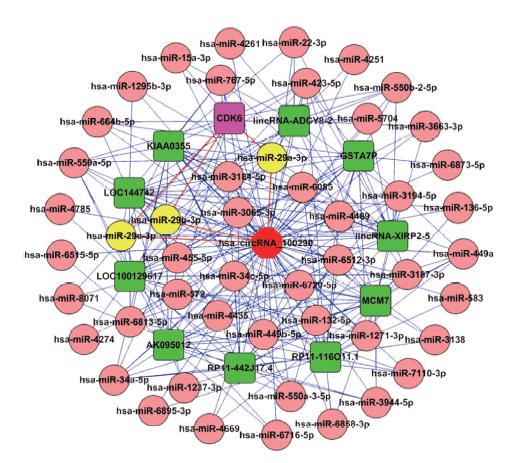
图2:ceRNA分析揭示circRNA_100290通过CeRNA机制调控CDK6
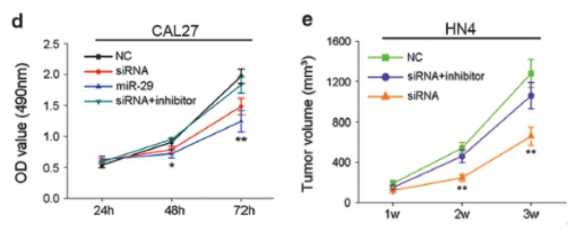
图3:in vitro和in vivo验证circRNA影响细胞的增殖
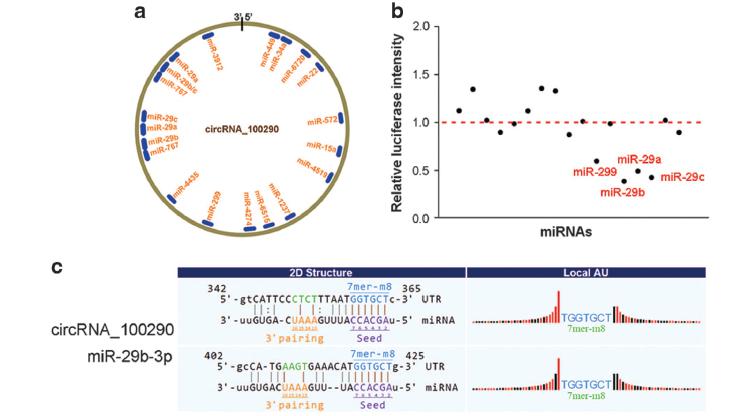
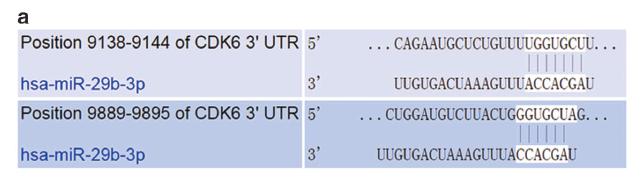

图4:Luciferase和EGFP/RFP reporter assays验证miR-29直接结合circRNA_100290/CDK
研究意义
研究揭示了circRNA_100290通过内源竞争结合miR-29,调控CDK6基因的表达,进而影响口腔鳞状细胞癌的增殖,可以作为OSCC的治疗的潜在靶点。
作者介绍
陈林,博士,中南大学湘雅二医院口腔颌面外科副主任医师。长期从事口腔颌面外科临床及研究工作,对口腔癌的预防及治疗有丰富经验,至今已发表与口腔临床相关的文章数十篇。
论文链接
circRNA_100290 plays a role in oral cancer by functioning as a sponge of the miR-29 family.
http://www.nature.com/onc/journal/vaop/ncurrent/full/onc201789a.html
